Co je bakteriofágy?
Obsah
- Příběh
- Bakteriofágy v přírodě
- Klasifikace
- Jaké problémy řeší bakteriofágové přípravky?
- Bakteriofágový akční mechanismus
- Dvě strany medaile
- aplikace

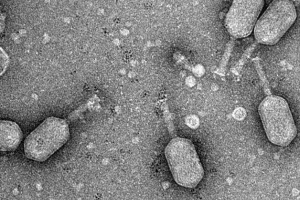
Bakteriofágy nebo fágy (od dr.-Grech. ᾰᾰγΩ - "Devout") - viry, selektivní ovlivňující bakteriální buňky. Nejčastěji bakteriofágy násobí uvnitř bakterií a způsobují jim lýzu. .
Příběh
Anglický bakteriolog Frederick Tores V článku 1915 popsal infekční onemocnění Staphylococci, infekční činidlo prošlo filtry a mohlo by být přeneseno z jedné kolonie na druhou. Bez ohledu na Frederick Tore, francouzsko-kanadský mikrobiologa Felix D`Elell dne 3. září 1917 oznámil otevření bakteriofágů. Spolu s tím je známo, že ruský mikrobiolog Nikolai Fyodorovich Gamalei v roce 1897 poprvé pozoroval fenomén lýzových bakterií (Sybriced Stick) pod vlivem transfektovaného činidla.
Po otevření jevů bakteriofágu, D`Elell vyvinul doktrínu, že bakteriofágy patogenních bakterií, které jsou jejich paraziti, hrají velkou roli v patogenezi infekcí, což zajišťuje obnovu organismu pacienta a pak vytváří specifickou imunitu. Tato situace přilákala pozornost mnoha výzkumných pracovníků na fenomén bakteriofágu, který měl najít důležité prostředky boje proti nejnebezpečnějším infekčním onemocněním člověka a zvířat v fágech. Také Felix d`Elell předložil předpoklad, že bakteriofágy mají korpuskulární povahu. Nicméně, pouze po vynálezu elektronového mikroskopu se podařilo vidět a prozkoumat ultrastrukturu fugy.
Bakteriofágy v přírodě
Bakteriofágy jsou neviditelně přítomny všude v našem světě - v oceánu, půdě, zdroje hlubokých vod, pitné vody a potravin. Jsou to nejvíce prezentovaná forma života na Zemi - od 10třicet na 1032 fágové částice v biosféře - a hrají klíčovou roli při zachování zůstatku všech studovaných ekosystémů. Bakteriofágy jsou přírodní regulátory a bojovníci s bakteriemi a poskytují dynamickou rovnováhu v přírodě, při zachování relativní stálosti mikrobiální krajiny v přírodě a omezení růstu bakterií obyvatelstva. Bakteriofágy jsou přítomny i v našem jídle - denně jíst bakteriofágy s jídlem, ve kterých jsou přítomny přirozeně, reguluje mikrobiální rovnováhu v lidském těle.
Slavný vědec D, Erell představil světu bakteriofágů jako přírodních antibakteriálních činidel a nabídl je použít pro terapii - ještě před otevřením antibiotik.

Klasifikace
Dvě skupiny bakteriofágů rozlišují: Mírný a virulentní. Střední fágy pomalu násobí uvnitř postižené bakteriální buňky, jsou přenášeny uvnitř bakteriální kolonie z generace na generaci, periodicky ničí mikrobiální buňky. Takový účinek se nazývá lysogenní. Veselé fágy, zasáhnou mikrobuní kleci, začnou se rychle násobit, což vede k rychlé smrti infikované buňky. Takový účinek se nazývá litic.
Jaké problémy řeší bakteriofágové přípravky?
jeden.Efektivní boj s bakteriálními infekcemi
Vám umožní účinně řešit bakteriální infekce bez rizika rozvoje komplikací pro játra, ledviny a další životně důležité orgány vystavené škodlivým účinkem běžných antibakteriálních činidel.
2.Posílení působení antibiotik
Při použití s antibiotikem může účinnost druhé zvýšit.
3.Zničte jen škodlivé bakterie
Zničte škodlivé bakterie a uchovávejte své vlastní, "užitečné" bakterie pro nás (střevní mikroflóra, mikroflóna genitálních orgánů), bez způsobení dysbakteriózy.
4.Efektivní výměna antibiotik
.
5. Minimálně kontraindikace
V přítomnosti kontraindikací k použití antibiotik (s antibiotikem souvisejícím průjmem, porušením jater a ledvin atd.) - Bakteriofágy jsou nepostradatelné.
6. Bakteriofágy mohou být použity jak uvnitř, tak pro venkovní použití
Bakteriofágy mohou být použity jak dovnitř a použity pro venkovní použití, které řeší problém nejen na úrovni celého těla, ale také lokálně v lokalizačním místě infekce.
Bakteriofágový akční mechanismus

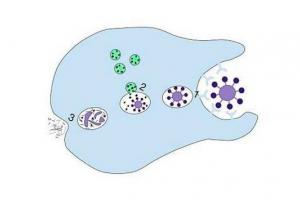
Virus proniká do buňky patogenní bakterie, zavedený do svého genomu a začíná se množit. Po akumulaci uvnitř bakteriální buňky určitého počtu nových virových částic (virionů) je buňka zničena, viry outpace a infikovat nové bakteriální buňky.
Životní cyklus bakteriofágu
- FAG se přiblíží bakterie a ocasní nitě jsou spojeny s receptorovými oblastmi na povrchu bakteriální buňky.
- Ocasní nitě jsou ohnuté a "bodové" hroty a bazální deska na povrchu buněčného pouzdra se sníží, což nutí dutou tyč vstoupit do buňky, která má být usnadněna enzymem lizomim, který je v bazální desce, nukleové kyseliny (DNA nebo RNA) je zavedena uvnitř buňky.
- Nukleic fágová kyselina kóduje syntézu fágových enzymů s použitím hostitelského šéfa.
- Phag inaktivuje DNA a RNA majitele a fágové enzymy zcela rozdělují svůj fágový RNA podřízený buněčný přístroj.
- Nukleová kyselina fága je replikována a kóduje syntézu nových plášťových proteinů.
- Nové fágové částice tvořené v důsledku spontánní samo-montáže proteinového pláště kolem fágu nukleové kyseliny, pod kontrolou syntetizovaného lysozymu fágového fága RNA.
- Lisace Buňky: Buňka praskla pod vlivem lysozymu- je propuštěn asi 200 až 200-1000 nových fázových fází infikují další bakterie.
- Fáze 1-7 v čase zabírají asi 30 minut - toto období se nazývá latentní období.
Dvě strany medaile
Výhody
Bakterie ztrácejí citlivost na působení antibiotik. Farmaceutický průmysl je neúnavně syntetizuje ostatní. Je však známo, že možnosti syntézy antibiotik jsou omezené. K působení bakteriofágů Antibiotika se přizpůsobí velmi tvrdě a podle odborníků se mikroby nemohou vyvinout odolnost vůči komplexu několika bakteriofýgů;. Kromě toho, bakteriofágy prakticky nemají vedlejší účinky, alergické jevy jsou méně časté, mohou být kombinovány s jakýmikoliv léků. Bakteriofágy v tuto chvíli se ukázaly jako při léčbě urologických onemocnění, hnisavé procesy v chirurgii, jakož i při léčbě střevní infekčních onemocnění u novorozenců.
nevýhody
- Bohužel, nedostatky lékařských bakteriofýgů také hodně. Nejdůležitějším problémem vychází z důstojnosti - vysoká specifičnost fágů. Každá bakteriofága infikuje přísně definovaný typ bakterií, ani taxonomický vzhled, ale řada užších odrůd, kmenů. . Proto pro aktuální fágové přípravky existují případy neefektivních aplikací. Lék vyrobený proti určité sadě kmenů a dokonale navštěvující Streptococccal angina v Smolensku může být bezmocný proti všem známkám téže anginy v Kemerovo. Onemocnění je stejná, způsobená stejným mikrobem a kmeny streptokoků v různých oblastech, které se odlišují.
Pro nejefektivnější použití bakteriofágu je nutná přesná diagnóza patogenního mikrobu, až k napětí. Nejčastějším způsobem diagnostiky - setí kultury - trvá spoustu času a požadovaná přesnost nedává. Rychlé metody - psaní s polymerázovou řetězovou reakcí nebo hmotnostní spektrometrií - jsou zavedeny pomalu v důsledku vysokých nákladů na vybavení a vyšší kvalifikaci pro laboratorní techniky. V ideálním případě by výběr složek PHAS léčiva mohl být proveden proti infekci každého konkrétního pacienta, ale je to drahé a v praxi nepřijatelné.
- Dalším důležitým nedostatkem fágů - jejich biologická povaha. Kromě toho, že bakteriofágy pro udržování infekci vyžadují zvláštní podmínky pro skladování a přepravu, takový způsob léčby otevírá prostor pro různé spekulace na téma "Zahraniční DNA v člověku". .
- . If the microbial infection develops there, where the bacteriophage can be applied directly in the form of droplets, spray, or enema, - on the skin, open wounds, burns, nasopharmal sheaths, ears, eyes, and a large intestine - then there are žádné problémy.
- Pokud však dojde k infekci ve vnitřních orgánech, je situace obtížnější. Případy úspěšného vyléčení ledvin nebo slezin infekcí s obyčejným perorálním podáváním přípravy bakteriofágu jsou známy. Mechanismus penetrace je však poměrně velký (100 nm) fágové částice ze žaludku v krevním řečišti a ve vnitřních orgánech jsou chápány špatně a budou velmi od pacienta k pacientovi. Bakteriofágy jsou bezmocné a proti těm mikrobům, které se vyvíjejí uvnitř buněk, jako je tuberkulóza a lepry. Přes stěnu lidské buňky, bakteriofág se nemůže dostat.
Je třeba poznamenat, že by neměl být proti použití bakteriofágů a antibiotik pro lékařské účely. S jejich společnou akcí je pozorován vzájemný nárůst antobakteriálního účinku. To umožňuje například snížit dávku antibiotik na hodnoty, které nezpůsobují vyslovované vedlejší účinky. Mechanismus vývoje bakterií stability na oba složky kombinovaného léku je tedy téměř nemožný.
Rozšíření arzenálu antimikrobiálních léčiv poskytuje více stupňů svobody ve výběru léčebné techniky. Vědecky založený vývoj konceptu použití bakteriofágů v antimikrobiální terapii je tedy perspektivní směr. Bakteriofágy nejsou příliš alternativní jako přídavek a posílení v boji proti infekcím.

aplikace
V medicíně
Jednou z oblastí použití bakteriofágů je antibakteriální terapie, alternativní přijetí antibiotik. Používají se například bakteriofágy: streptokoková, stafylokoková, pebesielóza, dysenterický polyvalent, piobacteriofage, jestliže, protein a quiprotane a další. V současné době se používají k léčbě bakteriálních infekcí, které nejsou citlivé na tradiční léčbu antibiotiky, zejména v Gruzii republiky. . Terapeutické použití bakteriofágů nedostalo schválení na západě, i když fagy platí pro zničení bakterií způsobujících otravu potravin, jako jsou licence. V mnoha obdobích zkušeností v objemu velkého města a venkovských oblastí byla prokázána neobvykle vysoká terapeutická a preventivní účinnost dysenterické bakteriofágy.
V biologii
Bakteriofágy se používají v genetickém inženýrství jako vektory přenášení DNA a přirozené převodovky mezi bakteriemi přes některé fágy (transdukce).
Fágové vektory jsou obvykle vytvářeny na základě mírné bakteriofágy λ, obsahující dvouvláknovou lineární molekulu lineární DNA. Levá a pravá ramena fága mají všechny geny potřebné pro litický cyklus (replikace, reprodukce). Střední část genomu bakteriofága λ (obsahuje geny řízení leasingu, tj. Její integrace do DNA bakteriální buňky) není nezbytná pro jeho reprodukci a je přibližně 25 tisíc párů nukleotidů. Tato část může být nahrazena zahraničním fragmentem DNA. . Vektory na bázi bakteriofágu λ se používají k klonování fragmentů DNA eukaryotes (to jsou větší geny) až 23 tisíc párů nukleotidů (t. P. N.). A fágy bez vložek jsou menší než 38 tun. P. N. nebo, naopak s příliš velkými vložkami - více než 52 tun. P. N. nevyvíjí se a neovlivňují bakterie.
Protože reprodukce bakteriofágu je možná pouze v živých buňkách, mohou být bakteriofágy použity k určení životaschopnosti bakterií. Tato oblast má velké perspektivy, protože jedna z hlavních otázek v různých biotechnologických procesech je stanovení životaschopnosti použitých kultur. Použití způsobu elektroopetické analýzy buněčných suspenzí, možnost studia fází interakce fágové mikrobiální buňky.